| [Türkçe] | |
|
 |
| Turkish Society of Cardiology Cardiooncology Bulletin Year: 1 Number: 3 / 2023 |
|
Avrupa Kardiyoloji Derneği (ESC), Avrupa Hematoloji Derneği (EHA), Avrupa Terapötik Radyoloji ve Onkoloji Derneği (ESTRO) ve Uluslararası Kardiyo-Onkoloji Derneği (IC-OS) işbirliği ile hazırlanmış 2022 Kardiyo-Onkoloji Kılavuzu – Antrasiklin ve HER2 Hedefli Tedavi İlişkili Kardiyotoksisite 2022 ESC Guidelines on cardio-oncology developed in collaboration with the European Hematology Association (EHA), the European Society for Therapeutic Radiology and Oncology (ESTRO) and the International Cardio-Oncology Society (IC-OS) – Anthracycline and HER2 Targeted Therapy Related Cardiotoxicity Dr. Yusuf Ziya ŞENER Hacettepe Üniversitesi Tıp Fakültesi, İç Hastalıkları Anabilim Dalı Antrasiklin Kardiyotoksisitesi Antrasiklinler; meme kanseri, mide kanseri, sarkomlar ve hematolojik maligniteler başta olmak üzere pek çok kanser türünde kullanılmaktadır. Antrasiklinler, topoizomeraz 2ß inhibisyonu yoluyla mitokondriyal aktiviteyi inhibe ederek ve hücre ölümünü tetikleyerek kardiyotoksisiteye neden olurlar. Antrasiklin kardiyotoksisitesi kümülatif doz ile ilişkilidir ve kardiyotoksisite genellikle geri dönüşsüzdür. Antrasiklin toksisitesinin, ilaç alınırken akut dönemde gelişebileceği gibi 10 yıl kadar sonra bile ortaya çıkabileceği unutulmamalıdır. Başlıca kullanılmakta olan antrasiklinler; doksorubisin, epirubisin, daunorubisin, mitoksantron ve idarubisindir. Antrasiklinlerin kardiyotoksisite riski için doz oranları Tablo 1’de özetlenmiştir.
Antrasiklin tedavisi planlanan hastada öncelikle bazal kardiyovasküler (KV) risk belirlenmelidir. Düşük ve orta KV risk grubundaki hastalarda tedavi başlanması ve Onkoloji takibinde kardiyotoksisite şüphesi gelişmesi halinde hastanın Kardiyoloji bölümüne yönlendirilmesi önerilmektedir. Yüksek ve çok yüksek KV risk grubundaki hastalarda ise tedavi öncesinde hastanın Kardiyoloji bölümüne yönlendirilmesi ve Kardiyoloji ile birlikte tedavi sürecinin yönetilmesi önerilmektedir. Yüksek ve çok yüksek KV risk grubunda aynı zamanda tedavi sürecinde toksisiteden primer korunma amacı ile anjiyotensin dönüştürücü enzim (ACE) inhibitörleri ya da anjiyotensin reseptör blokörleri (ARB) ve statin tedavisinin eklenmesi Sınıf 2a olarak kılavuzda önerilmektedir. Ayrıca daha az toksik bir form olan lipozomal doksorubisin, yüksek ve çok yüksek KV riski olan hastalarda ve uygun kanserlerde (Metastatik meme kanseri, over kanseri, HIV ilişkili Kaposi sarkomu ve multipl myelom) tercih edilebilir. Deksrazoksan ise bir demir şelatörüdür ve antrasiklin kardiyotoksisitesini önleyici etkileri mevcuttur. Yüksek ve çok yüksek KV riski olan hastalarda, özellikle kümülatif dozun 300 mg/m2’yi geçtiği metastatik meme kanseri hastalarında kullanılması düşünülmelidir. Deksrazoksan, her kemoterapiden yarım saat önce infüzyon şeklinde, deksrazoksan/doksorubisin doz oranı 10:1 olacak şekilde verilmelidir. Antrasiklin öncesi KV risk değerlendirmesi Tablo 2’de özetlenmiştir.
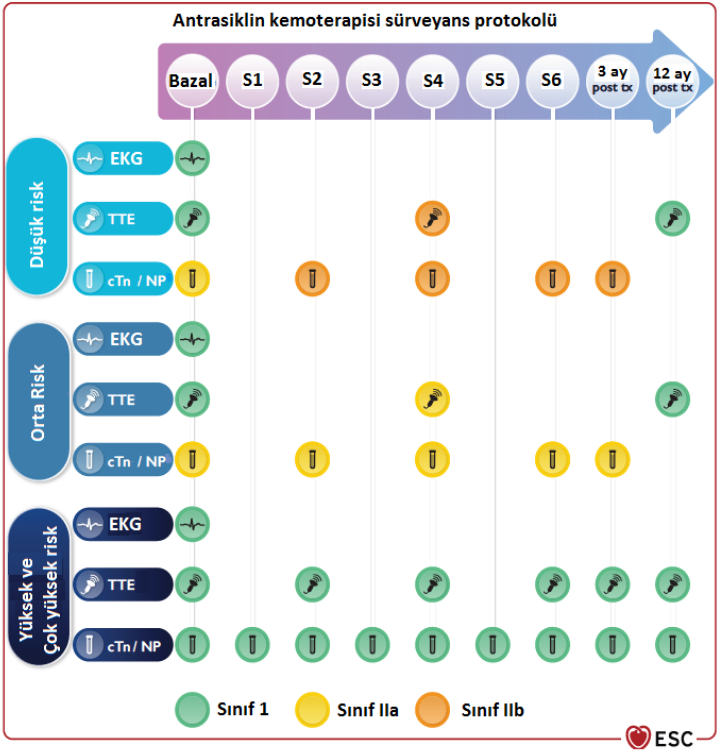
Antrasiklin tedavisi başlanacak bütün hastalardan tedavi öncesinde bazal kardiyak troponin ve natriüretik peptid ölçümü yapılması, elektrokardiyografik ve ekokardiyografik değerlendirme yapılması önerilmektedir. Bu ölçümlerin KV risk grubuna göre belirli aralıklarla tekrar edilmesi gerekmektedir. Antrasiklin tedavisi sırasında toksisite sürveyans takibi Şekil 1’de özetlenmiştir. Antrasiklin tedavisi tamamlandıktan 3 ay ve 12 ay sonra da kardiyak belirteç ve ekokardiyografik değerlendirme yapılması önerilmektedir. Kardiyotoksisite takibinde birinci basamakta önerilen görüntüleme yöntemi ekokardiyografidir. Mümkünse 3D-ekokardiyografik ölçümle ejeksiyon fraksiyonu değerlendirilmelidir. Kardiyotoksisite takibinde, erken tanıya olanak sağlaması nedeni ile global longitudinal strain (GLS) değerlendirmesi yapılmalıdır. GLS değerinde >%15 azalma olması kardiyotoksisite açısından tanısaldır. Sol ventrikül ejeksiyon fraksiyonunda (EF) azalma strain değişikliğinden daha sonra ortaya çıkar. Takipte EF değerinde > %10 azalma ile birlikte değerin %50’nin altına inmesi antrasiklin kardiyotoksisitesi için tanısal kabul edilmektedir. Ekokardiyografik görüntü kalitesi kötü olan hastalarda kardiyak MR ile ejeksiyon fraksiyonu ve strain değerlendirmesi düşünülmelidir. MUGA sintigrafisi de toksisite tanı ve tedavisinde alternatif bir görüntüleme yöntemidir. Antrasiklin kardiyotoksisitesi gelişme zamanına göre akut, erken ve geç olarak sınıflandırılmaktadır. Akut toksisite, infüzyondan hemen sonra gelişir, genellikle geridönüşlüdür, EKG değişikliği, aritmi ve kardiyak belirteç yüksekliği ile karakterizdir. Erken toksisite, antrasiklin tedavisinden sonraki 1 yıl içerisinde gelişen toksisitedir. Geç toksisite ise tedavi bittikten 1 sene sonrasındaki dönemde gelişen toksisite olarak tanımlanmaktadır. Semptom varlığına ve sistolik fonksiyon bozukluğuna göre kardiyotoksisite sınıflandırması Tablo 3’te özetlenmiştir.
Şekil 1. Antrasiklin kemoterapisi alan hastalarda kardiyotoksisite takip şeması Kısaltmalar: S1: Birinci siklus, Post tx: Tedavi sonrası, EKG: Elektrokardiyografi, TTE: Transtorasik ekokardiyografi, cTn: Kardiyak troponin, NP: Natriüretik peptit
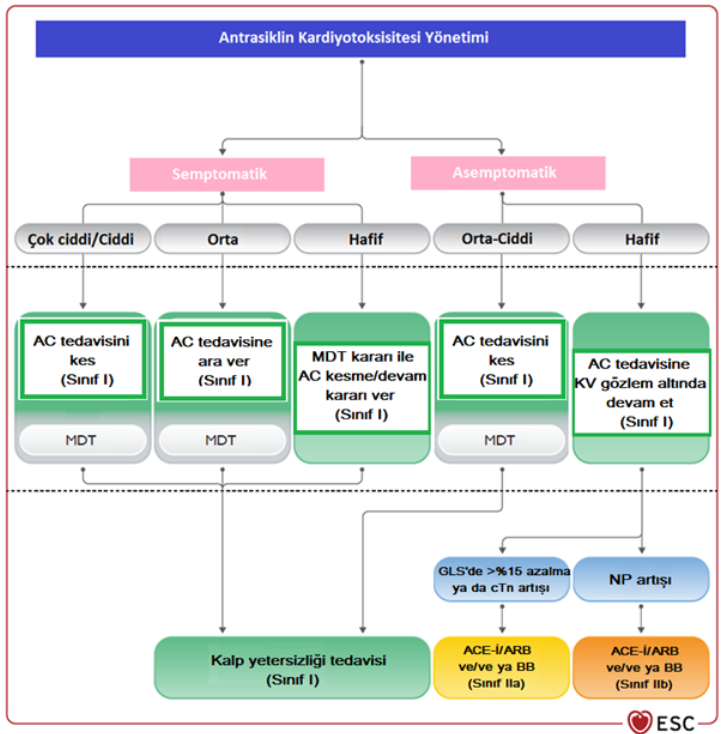
Antrasiklin toksisitesi geliştiğinde antrasiklin tedavisine devam kararı toksisite ciddiyetine göre değişmektedir. Ciddi ve çok ciddi semptomatik toksisitede antrasiklin kalıcı olarak kesilmeli ve antrasiklin tedavisinin ancak ve ancak alternatif tedavi olmayan durumlarda, kardiyak fonksiyonlar düzeldikten sonra multidisipliner ekibin kararına göre ve koruyucu önlemler alınarak (doz azaltımı, lipozomal formülasyon kullanımı, deksrazoksan verilmesi vb.) tekrar başlanması düşünülmelidir. Orta derece semptomatik, orta ve ileri derece asemptomatik toksisite gelişen vakalarda antrasiklin tedavisi geçici olarak durdurulmalıdır ve toksisite düzeldikten sonra lüzum halinde gerekli önlemler alınarak tekrar başlanmalıdır. Hafif toksisite gelişen vakalarda antrasiklin tedavisine ara verilmesine multidisipliner takım değerlendirmesi ile karar verilmelidir. Semptomatik bütün olgularda ve asemptomatik orta ve ciddi derecede toksisite gelişen vakalarda kılavuz bazlı kalp yetersizliği tedavisi (RAS blokörü + beta blokör+ mineralokortikoid reseptör antagonisti + SGLT2 inhibitörü) başlanmalıdır. Hafif asemptomatik toksisite gelişen hastalara RAS blokörü ve beta blokör kombinasyonu başlanması düşünülebilir. Antrasiklin toksisitesi gelişen hastalara aerobik egzersiz de önerilmelidir. Antrasiklin ilişkili kardiyotoksisite yönetimi Şekil 2’de özetlenmiştir.
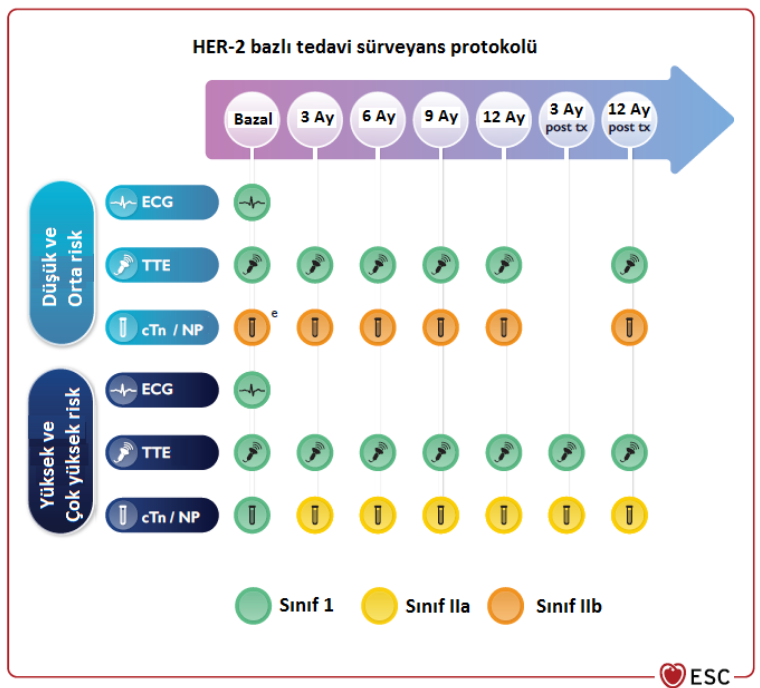
Şekil 2. Antrasiklin kardiyotoksisitesi yönetimi Kısaltmalar: AC: Antrasiklin, KV: Kardiyovasküler, MDT: Multidisipliner takım, GLS: Global longitudinalstrain, cTn: Kardiyak troponin, NP: Natriüretik peptit, ACE-İ: ACE inhibitörü, ARB: Anjiyotensin reseptör blokörü, BB: Beta blokör HER2 Hedefli Tedavi İlişkili KardiyotoksisiteHER2 hedefli tedaviler HER2 (+) meme kanseri ve proksimal mide kanseri tedavisinde kullanılmaktadır. En bilinen HER2 hedefli tedavi trastuzumab olmakla birlikte; pertuzumab, neratinib, lapatinib ve tucatinib gibi başka ajanlar da mevcuttur. Antrasiklin toksisitesinden farklı olarak, HER2 hedefli kardiyotoksisite doz bağımlı değildir ve ilaç kesildikten sonra toksisite genellikle geridönüşlüdür. Eş zamanlı antrasiklin kullanımı ve göğüs bölgesine radyoterapi uygulaması HER2 hedefli tedavi ilişkili kardiyotoksisite gelişme riskini artırmaktadır. Hastanın ek olarak antrasiklin tedavisi de alması gerekiyor ise antrasiklin ve HER2 hedefli tedavinin eş zamanlı verilmesinden ziyade ardışık olarak verilmesi tercih edilmelidir. HER2 hedefli tedavi başlamadan önce hastanın kardiyovasküler riski değerlendirilmelidir (Tablo 2). HER2 hedefli tedavi başlamadan önce, hastalardan bazal kardiyak troponin ve natriüretik peptid düzeyi çalışılmalı, EKG ve ekokardiyografik değerlendirme yapılmalıdır. HER2 hedefli tedavi alan hastalarda da hastaların KV risk durumuna göre belirli aralıklarla kardiyak belirteç, EKG ve ekokardiyografi takibi yapılmalıdır. HER2 hedefli tedavi ilişkili kardiyotoksisite tespitinde natriüretik peptid ölçümünün troponin ölçümüne göre daha hassas olduğu bildirilmiştir. HER2 hedefli tedavi tamamlandıktan sonraki 3. ve 12. ayda da hastanın bazal KV riskine göre kardiyak belirteç ve ekokardiyografi değerlendirilmesi yapılmalıdır. HER2 hedefli tedavi sürecindeki kardiyotoksisite sürveyansı Şekil 3’te gösterilmiştir.
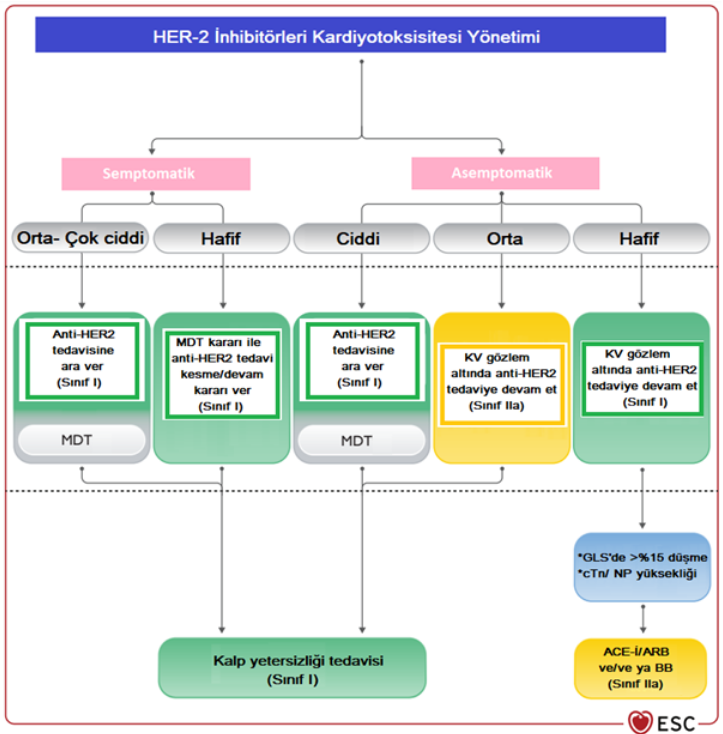
Şekil 3. HER-2 hedefli tedavi alan hastalarda kardiyotoksisite takip şeması Kısaltmalar: Post tx: Tedavi sonrası, EKG: Elektrokardiyografi, TTE: Transtorasik ekokardiyografi, cTn: Kardiyak troponin, NP: Natriüretik peptit HER2 hedefli tedavi ilişkili kardiyotoksisite sınıflandırması antrasiklin toksisitesi ile aynı olup Tablo 3’de özetlenmiştir. Semptomatik kalp yetersizliği varlığında hafif evre dışında anti-HER2 tedaviye ara verilmelidir. Hafif evre semptomatik vakalarda ise multidisipliner Kardiyo-onkoloji ekibinin kararına göre hareket edilmelidir. Asemptomatik ciddi kardiyotoksisite varlığında ilaç kesilmelidir ancak orta ve hafif asemptomatik kardiyotoksisitede ACE-i/ARB ve beta blokör tedavi kombinasyonu altında anti-HER2 tedaviye yakın gözetim altında devam edilebilir. Ciddi asemptomatik ve orta ve üzeri semptomatik toksisite gelişen ve HER2 hedefli tedavi kesilen hastalarda sol ventrikül fonksiyonları düzeldikten sonra hastanın tedavi endikasyonuna ve multidisipliner ekibin kararına göre HER2 hedefli tedaviye tekrar başlanabilir. HER2 hedefli tedavi ilişkili kardiyotoksisite yönetimi Şekil 4’te özetlenmiştir.
Şekil 4. HER2 inhibitörü kardiyotoksisitesi yönetimi Kısaltmalar: KV: Kardiyovasküler, MDT: Multidisipliner takım, GLS: Global longitudinalstrain, cTn: Kardiyak troponin, NP: Natriüretik peptit, ACE-İ: ACE inhibitörü, ARB: Anjiyotensin reseptör blokörü, BB: Beta blokör |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2026 © Turkish Society of Cardiology. |