|
| PH Gündem Yıl: 2018 Sayı: 3 |
|
Dr. Ebru Özpelit, Prof. Dr. Bahri Akdeniz Tanım ve Morfoloji: İlk kez 1888 yılında Etienne-LouisArthur Fallot, hastalığı Maladie Bleue (blue disease) olarak tanımlamış ve sorumlu olan 4 anatomik patolojiyi tariflemiştir1. Bunlar: 1-Geniş VSD Aslında tüm bu patolojilerin altında yatan tek bir gelişimsel anomali vardır; interventriküler septumun infundibuler kısmının (conal septum) , musküler septuma göre anterior deviasyonu (Şekil 1).
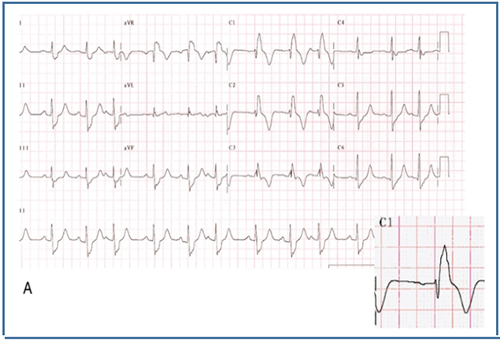
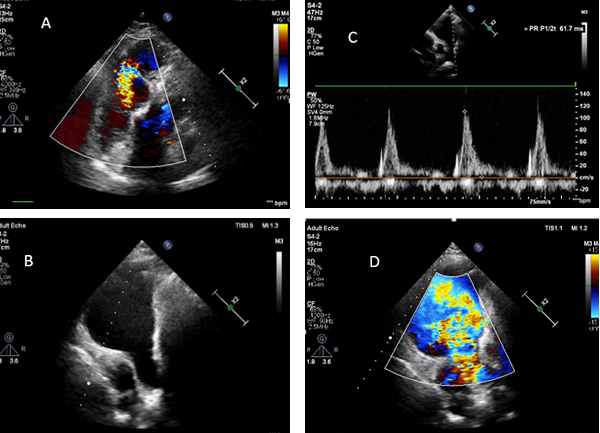
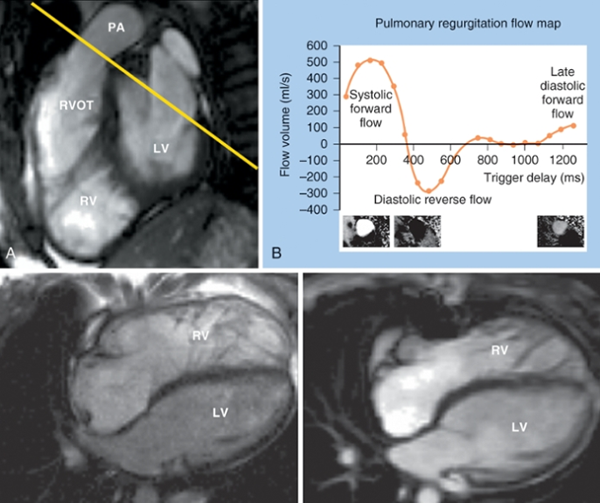
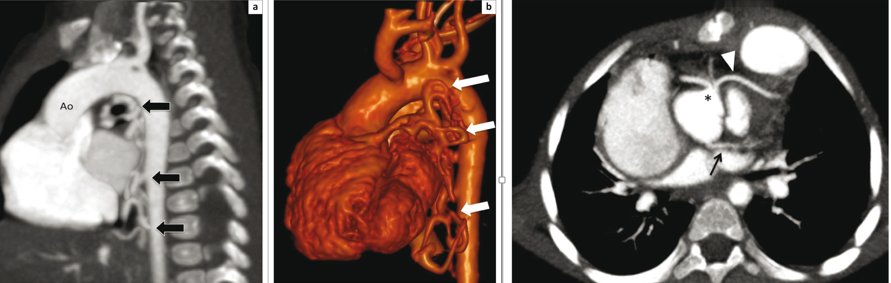
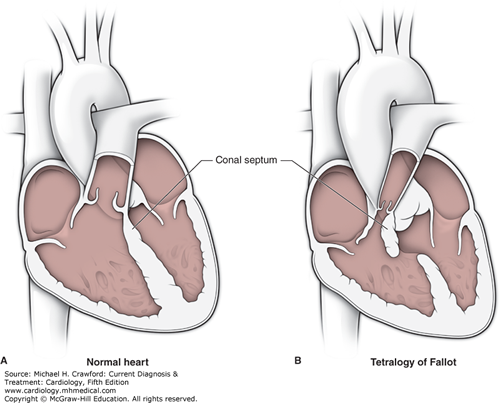 Şekil 1: TOF’un anatomik bulgularından sorunlu olan infundibüler septumun anterior deviasyonu Bu deviasyonun derecesine göre, bulgular geniş bir spektrumda ortaya çıkabilir. İntrakardiyak patolojiler, hastalarda çoğunlukla benzer karakterde olsa da, RVOT darlığı çok hafiften (pembe TOF), komplet pulmoner kapak atrezisine kadar farklı derecelerde olabilmektedir. Olguların %50’ine, pulmoner arter hipoplazisi ya da pulmoner arter dallarından birinin (tipik olarak sol dalın) komplet agenizisi eşlik etmektedir2. Eşlik eden diğer anomaliler arasında ASD ve koroner arter anomalileri en sık gözlenilenlerdir. Olguların %3’ünde bildirilen, sağ çıkışlı LAD, RVOT’u çaprazlayarak sola geçtiği için, cerrahi planlamada önem arz etmektedir2. Bu hastalarda RVOT darlığına müdahale için sağ ventrikül ve pulmoner arter arasına kondüit bağlanması gerekli olabilmektedir. Genetik ve Epidemiyoloji: Erişkin Dönemde Klinik Prezentasyon: Cerrahi prosedürler: Başarılı düzeltici ameliyat sonrasında survi bu hastalarda oldukça iyidir, 36 yıllık survi %85 oranında bildirilmiştir5,6. Ameliyat edilmiş erişkin hastalar, dispne, çarpıntı , senkop ya da ani kardiyak ölüm ile prezente olabilir. Bu klinik prezentasyonlara sebep olabilecek pek çok postoperatif komplikasyon mevcuttur. Bu komplikasyonları tanımak, tedaviyi doğru yönlendirmek için en temel şarttır. Dolayısıyla erişkin dönemde herhangi bir nedenle başvurmuş, opere TOF hastasını değerlendirirken , aşağıdaki postoperatif komplikasyonlar, akılda tutulmalı ve taranmalıdır. Postoperatif komplikasyonlar: Erişkin TOF hastasına klinik yaklaşımımız nasıl olmalı? Bu olası postoperatif komplikasyonları taramada fizik muayene, EKG, EKO, egzersiz testleri, Holter EKG, kardiyak MR, kardiyak BT , kardiyak kateterizasyon ve EPS , şüphenilen duruma göre kullanılabilecek tanısal testlerdir. Fizik muayenede sağ kalp yetmezliği bulguları, saturasyon ve üfürümler değerlendirilmelidir. EKG’de sıklıkla sağ dal bloğu ve sağ ventrikül hpertrofisi görülebilmektedir. (Şekil 2) QRS süresi ve QRS fragmentasyonu bu hastalarda mutlaka değerlendirilmelidir. Çünkü QRS süresinin ≥180msn olması ve fragmente QRS varlığı ani kardiyak ölüm açısından risk prediktörü olarak kabul edilmektedir7,8. Yine hastalar hem atriyal hem de ventriküler taşikardiler yönünden Holter EKG ile taranmalıdır. Egzersiz testleri ile hastaların fonksiyonel sınıf değerlendirmesi ve egzersiz kapasiteleri değerlendirilmelidir. Bu amaçla 6 dakika yürüme testi ya da daha ideal olarak kardiyopulmoner egzersiz testleri kullanılabilmektedir. Ekokardiyografide sağ ve sol ventrikül boyut ve fonksiyonları, sol ve sağ atrium boyutları, RVOT’da rezidüel darlık ve seviyesi, pulmoner, triküspit ve aortik kapak yetmezlikleri , rezidüel VSD varlığı, aort kökü boyutu , pulmoner arter basıncı, ana pulmoner arter ve dallarının devamlılığı ve kalibrasyonu, mutlaka değerlendirilmelidir.(Şekil 3) Kardiyak MR, opere TOF hastalarında sağ ventrikül boyut ve fonksiyonları ile pulmoner yetmezlik derecesini değerlendirmede ideal yöntemdir.(Şekil 4) Kardiyak BT ise, MR yapılamayan hastalarda ve de pulmoner arter dalları ile koroner arter anatomisinin değerlendirmesinde kullanılmaktadır.(Şekil 5) Tüm bu noninvaziv değerlendirmelerin sonuçsuz kaldığı hastalarda, hemodinamik değerlendirme amacı ile kardiyak kateterizasyon istenebilir. Aritmi yönünden şüphede kalınan hastalarda da EPS, istenebilecek bir diğer tanısal testtir.
Erişkin TOF hastası, bu testlerden gerekli olanlar ile değerlendirildikten sonra, tekrar bir müdahale gerekliliği yönünden irdelenmelidir. Erişkin hastada en sık reoperasyon nedenleri , pulmoner kapaktaki rezidüel darlık ve yetmezliklerdir. ESC 2010 eriişkinlerde konjenital kalp hastalıkları kılavuzuna göre, pulmoner darlık için asemptomatik hastada >80mmHg gradient, semptomatik hastada ise>60mmHg gradient müdahale endikasyonudur9. Anatomisi uygun hastada perkütan balon valvüloplasti ya da perkütan kapak replasmanı (Melody Valve) cerrahiye sıklıkla tercih edilmektedir10. Ancak müdahale gerektiren ciddi rezidüel pulmoner darlıklı olgu sayısı çok değildir. Ciddi pulmoner yetmezlik ise opere TOF hastasındaki en sıcak başlıktır. Çünkü özellikle transanüler yama uygulanan hastalarda sıkça görülmektedir. Bu hastalara hangi aşamada müdahale edilmesi gerektiği ise, oldukça tartışmalı bir konudur. Ciddi PY, 30 yaş öncesinde sıklıkla iyi tolere edilmektedir. Eşlik eden RV disfonksiyonu , pulmoner arter distal darlığı ya da pulmoner hipertansiyonu olan olgularda ise düşük debi bulgularına ve egzersiz kapasitesinde belirgin azalmaya sebep olabilmektedir11. Daha da önemlisi hastalarda geri dönüşümsüz RV disfonksiyonuna ve bununla ilişkili ani kardiyak ölümlere yol açabilmektedir11. Bu nedenle, hastalar asemptomatik dahi olsa RV’de belirgin genişleme ve disfonksiyon varsa ( RV sistol sonu hacim indeksi>80-90ml/m2 , RV diastol sonu hacim indeksi >150-160ml/m2 ) , pulmoner kapak replasmanı günümüzde önerilmektedir12,13. Yine hastada QRS süresi ≥180msn ve progresif genişleme mevcutsa , artmış ani kardiyak ölüm riski nedeniyle PVR öneren kaynaklar mevcuttur14. Ancak bu hastalarda genişlemiş bir RVOT olduğu için perkütan müdahele şansı her zaman olmamaktadır. Perkütan pulmoner kapak replasmanı günümüzde en fazla 29mm genişlikteki RVOT’lara uygulanabilmektedir. Cerrahi PVR’de ise, sağ ventrikül ve hasta, reoperasyon ile ilişkili risklere maruz kalmaktadır. Bunun da ötesinde pulmoner kapak replasmanı, her ne yöntemle yapılırsa yapılsın, uzun dönemde, kapak durabilitesi ve infektif endokardit yönünden risklidir. Bunlar da, PVR sonrası hastaları tekrarlayan müdahaleler ile karşı karşıya bırakmaktadır. Tüm bunların ötesinde PVR her ne kadar FK’da iyileşme sağlasa da , mortalite-RV disfonksiyonu ve aritmi yönünden faydası gösterilememiştir10. Özetle ciddi PY’li opere TOF hastasına ne zaman PVR yapılması gerektiği hala net cevaplanmış bir başlık değildir. Geç müdahale, kalıcı RV disfonksiyonu ve artmış ani kardiyak ölüm riskini taşırken, erken müdahalenin de tekrarlayan müdahaleler, cerrahi komplikasyonlar ve infektif endokardit gibi riskler taşıdığı unutulmamalıdır10. Opere TOF hastalarının erişkin yaştaki en sık hastaneye başvuru nedeni aritmilerdir. Hastaların yaklaşık 1/3’ünde atrial ya da ventriküler artimiler gözlenebilmektedir15. Bu hastaların %40’ında da birden fazla aritmi birlikte görülebilmektedir15. Aritmi riski ve tipini belirleyen en önemli etken, yapılan ameliyatın karakteridir. Atrial aritmilerden en sık, atrial reentran taşikardiler , atrial flatter ve atrial fibrilasyon görülmektedir. Atrial aritmiler , sıklıkla uzun süreli sistemik-pulmoner arter şantı olan olgularda yada atriotomi uygulanmış hastalarda görülmektedir. Bu hastalarda, elektriksel ablasyon tercih edilen tedavi yöntemidir. Opere TOF hastalarında sıklıkla görülen bir diğer aritmi ise ventriküler taşiaritmilerdir. Özellikle ventrikülotomi uygulanmış hastalarda, skar dokusu ile ilişkili olarak reentran tarzda ventriküler taşikardiler gözlenebilmektedir. Ventriküler taşikardinin klinikteki en önemli prediktörü QRS genişlemesidir. QRS ≥180msn olması, QRS fragmentasyonu, >60msn QT dispersiyonu, QRS süresinde ameliyat sonrası progresif uzama ve belirgin RV ve LV disfonksiyonu ventriküler aritmi açısından en önemli risk faktörleridir15. Ciddi PY ile ventriküler aritmiler arasında belirgin bir korelasyon olsa da, PVR ile aritmi ve ani kardiyak ölümlerin azaltıldığı gösterilememiştir. Opere TOF hastalarında ölümlerin önemli bir nedeni, ani kardiyak ölümlerdir. Hastaların %0.5-%6’ında bildirilmiştir16. Ventriküler aritmi yönünden riskli bireylerde , EPS ile ventriküler stimulasyon yapılması önerilmektedir. EPS’de monomorfik VT indüklenen, ya da spontan VT’si saptanan hastalarda, hem ablasyon hem de profilaktik ICD implantasyonu sıklıkla önerilse de, günümüzde TOF hastalarında primer profilaksi amaçlı ICD endikasyonları tartışmalı konular arasında yerini korumaktadır. Özetle, erişkin dönemde TOF hastaları, bazal anatomik yapı ve uygulanan cerrahinin tipine göre farklı semptom ve bulgularla karşımıza çıkabilmektedir. Bu hastalarda olası postoperatif komplikasyonları bilmek ve hastaları bu açılardan doğru yöntemlerle taramak önemlidir. Özellikle rezidüel pulmoner kapak lezyonları ve artimiler erişkin dönemdeki en temel sorunlardır. Kaynaklar: 1-Hunter W. Medical observations and inquiries. London: Private publication, 1784: 417–19. 2- Gatzoulis MA: Diagnosis and management of adult congenital heart disease Third edition. Chapter 47:pages: 474-488 3-Apitz C, Webb GD, Redington AN. Tetralogy of Fallot. Lancet 2009;374(9699):1462–71. 4-Goldmuntz E, Clark BJ, Mitchell LE, et al. Frequency of 22q11 deletions in patients with conotruncal defects. J Am Coll Cardiol 1998; 32: 492–98. 5-Chiu SN, Wang JK, Chen HC, et al. Long-term survival and unnatural deaths of patients with repaired tetralogy of Fallot in an Asian cohort. Circ Cardiovasc Qual Outcomes 2012;5(1):120–5. 6. Bacha EA, Scheule AM, Zurakowski D, et al. Longterm results after early primary repair of tetralogy of Fallot. J Thorac Cardiovasc Surg 2001;122(1): 154–61. 7-M.A. Gatzoulis, J.A. Till, A.N. Redington: Depolarization-repolarization inhomogeneity after repair of tetralogy of Fallot. The substrate for malignant ventricular tachycardia?. Circulation95:401-404 1997 8-M.A. Gatzoulis, J.A. Till, J. Somerville, A.N. Redington: Mechanoelectrical interaction in tetralogy of Fallot. QRS prolongation relates to right ventricular size and predicts malignant ventricular arrhythmias and sudden death. Circulation. 92:231-237 1995 9-Baumgartner H, Bonhoeffer P, De Groot NM, et al. ESC guidelines for the management of grown-up congenital heart disease (new version 2010). Eur Heart J 2010;31:2915-57. 10- Bhagra CJ, Hickey EJ, Van De Bruaene A, et al. Pulmonary Valve Procedures Late After Repair of Tetralogy of Fallot: Current Perspectives and Contemporary Approaches to Management. Can J Cardiol. 2017 Sep;33(9):1138-1149. 11- Bouzas B, Kilner PJ, Gatzoulis MA. Pulmonary regurgitation: not a benign lesion. 12-Buechel ER, Dave HH, Kellenberger CJ, et al. Remodelling of the right ventricle after early pulmonary valve replacement in children with repaired tetralogy of Fallot: assessment by cardiovascular magnetic resonance. Eur Heart J 2005;26(24):2721–7. 13- Oosterhof T, van Straten A, Vliegen HW, et al. Preoperative thresholds for pulmonary valve replacement in patients with corrected tetralogy of Fallot using cardiovascular magnetic resonance. Circulation 2007;116(5):545–51 14- Uebing, D.G. Gibson, S.V. Babu-Narayan, et al.: Right ventricular mechanics and QRS duration in patients with repaired tetralogy of Fallot: implications of infundibular disease. Circulation. 116:1532-1539 2007 |
| 2026 © Bu sitenin tüm haklary Türk Kardiyoloji Derne?ine aittir. |